- Co je tepelná rovnováha?
- Co je tepelná rovnováha?
- Vzorec tepelné rovnováhy
- Nulový zákon termodynamiky
- Příklady tepelné rovnováhy
Vysvětlíme, co je tepelná rovnováha, z čeho se skládá a jaký je její vzorec. Také nulový zákon termodynamiky a příklady.
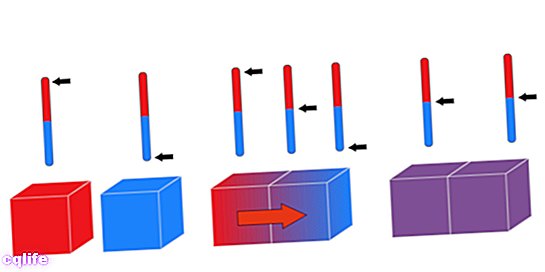
Co je tepelná rovnováha?
vfyzickýTepelná rovnováha se nazývá stav, ve kterém dvě tělesa, která jsou v kontaktu nebo jsou oddělena vodivým povrchem, vyrovnají své původně odlišné teploty v důsledku přenosu tepla z jednoho do druhého.
Pokud máme v kontaktu dva předměty, jeden teplejší než druhý, budou mít oba v průběhu času tendenci dosáhnout stejné teploty, a pokud nedojde k přenosu teplo vůči jiným objektům budou nadále udržovat tepelnou rovnováhu, tj teplota konstantní.
Co je tepelná rovnováha?

Tento jev lze vysvětlit mikroskopicky, přičemž se rozumí, že teplota objektů přímo souvisí s Kinetická energie průměr vašehočástice, býtatomy, molekulnebo ty, které je třeba vzít v úvahu. Tento průměr je to, co se ve fyzice běžně nazývá „vnitřní energie“, takže čím vyšší je kinetická energie, tím vyšší je vnitřní energie a tím vyšší je teplota systému.
Dvě tělesa v kontaktu si v průběhu času vyměňují energii. A tak je dosaženo bodu tepelné rovnováhy, když je kinetická energie obou těles stejná, takže obě tělesa začnou fungovat jako jediný termodynamický systém, obdařený stejným množstvím vnitřní energie a tedy i teploty.
Vzorec tepelné rovnováhy
Vyjádření tepelné rovnováhy zahrnuje výpočet teplotního rozdílu mezi dvěma tělesy, takže je třeba určit množství tepla (Q), které si vymění.
To se určí pomocí vzorce Q = m. Ce. Δt, kde m budeHmotnost těla, Ce suspecifické teplo vyjádřeno v cal / gr ° C, a Δt je změna teploty, to znamená: Δt = tf - ti, konečný čas mínus počáteční čas.
Jakmile je spočítáno teplo Q pro každé těleso, můžeme je porovnat s vědomím, že tepelná rovnováha nastává v rovnováze teplot mezi tělesem 1 a tělesem 2. K dosažení tepelné rovnováhy je zapotřebí teplo, které získá nejchladnější těleso. že nejteplejší těleso ztrácí, takže Q1 = Q2, tedy teplo získané = tepelné ztráty.
Nulový zákon termodynamiky
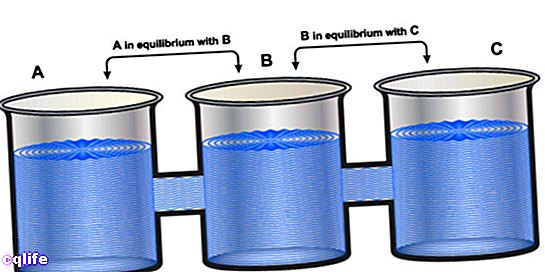
Tento princip je vyjádřen v tzv. nulovém zákoně termodynamiky, který v roce 1931 vyjádřil R. H. Fowler takto: „Pokud se najdou dva systémy A a B, každý zvlášť, v tepelné rovnováze s třetím Systém, který budeme nazývat C, pak A a B jsou také ve vzájemné tepelné rovnováze “.
To znamená: pokud A = C a B = C, pak A = B.
Díky tomuto principu, zaměřenému na matematickou formulaci termodynamiky, je známo, co Maxwell takto vyjádřil slovy: "Všechno teplo je stejného typu."
Příklady tepelné rovnováhy
Zde je několik jednoduchých příkladů tepelné rovnováhy:
- Když vstoupíme do teplé místnosti, vnímáme teplovzduch okamžitě, ale s určitou rezervoupočasí, naše tělo si vymění teplo se vzduchem a dostane se s ním do tepelné rovnováhy, takže přestaneme vnímat rozdíl teplot.
- Vložíme-li skleněnou nádobu se studenou vodou do větší nádoby s vroucí vodou, tepelný tok mezi nimi bude ochlazovat horkou vodu a ohřívat studenou, dokud nedosáhne střední úrovně tepelné rovnováhy.
- Výrobky, které máme v naší kuchyňské mrazničce, jsou v tepelné rovnováze s ohledem na zmrzlý vzduch mezi nimi, takže všechny sdílejí stejnou teplotu.
