Vysvětlíme, co je atom a jak se skládá každá z jeho částí. Také jeho historie, studie o něm a co je molekula.

co je atom?
Nejmenší jednotka, která tvoří hmota.
Slovo atom pochází ze starověké řečtiny (atom, "Bez dělení") a byl vytvořen prvními filozofy, kteří teoretizovali o složení věcí, tedy o elementárních částicích vesmír. Od té doby, se vznikem atomové modely, způsob jejich představování se nesmírně lišil, protože atomový model po staletí následoval předchozí, až jsme dospěli k tomu, který používáme dnes.
Atomy mají vlastnosti chemický prvek že skládají a prvky jsou organizovány a klasifikovány podle svých atomová čísla, elektronická konfigurace a chemické vlastnosti v Periodická tabulka prvků.
Stejný chemický prvek může být složen z různých atomů stejné třídy, to znamená se stejným atomovým číslem (počet protony které má každý atom v prvku), i když jejich atomové hmotnosti jsou různé.
Například existují různé atomy stejného prvku, které se liší počtem neutronya nazývají se izotopy, reprezentativním případem jsou izotopy prvku uhlík (12C, 13C, 14C). Takže každý atom patří ke stejnému chemickému prvku nebo ne, v závislosti na jeho počtu protonů, takže atomy se stejným počtem protonů patří ke stejnému chemickému prvku.
Jak se skládá atom?
Atomy se skládají z jádra a jednoho nebo více elektronů (které mají záporný náboj) kolem něj. Jádro je tvořeno částicemi zvanými protony a neutrony. Protony jsou kladně nabité a neutrony jsou neutrální. Soubor protonů a neutronů se nazývá nukleony.
Protony a elektrony jsou k sobě přitahovány elektromagnetickou silou (interakce nabitých částic s elektrickým a magnetickým polem), zatímco protony a neutrony jsou k sobě přitahovány jadernou silou (síla, kterou pociťují pouze částice, které tvoří atomové jádro).
Jak se atomy spojují?
Atomy se mohou vzájemně kombinovat a vytvářet chemické vazby, co se stane, když sdílejí své elektrony tak či onak. Chemické vazby mohou být kovalentní, iontový Y kovový, který vytváří kovalentní molekulární sloučeniny, iontové sítě nebo kovové sloučeniny (ačkoli je důležité objasnit, že žádná chemická vazba není absolutně kovalentní nebo iontová). Tímto způsobem se mohou atomy spojovat a vytvářet molekul jednoduché jako Voda, jakož i tvořit makromolekuly komplexní jako protein, DNA Y RNA.
Přestože se atomy od sebe odlišují díky konfiguraci svých částic, je také pravda, že všechny atomy téhož prvku jsou naprosto totožné: atomy vodíku v slunce Jsou stejné jako ty, které tvoří naše tělo, a atomy uhlíku v těle psa jsou totožné s těmi, které tvoří diamant. Rozdíl je ve způsobu, jakým se atomy spojují, aby vytvořily různé chemické sloučeniny, které tvoří orgány a orgánové systémy v žíjící bytosti, materiály generované v průmysla veškerá hmota, která tvoří vesmír.
Části atomu
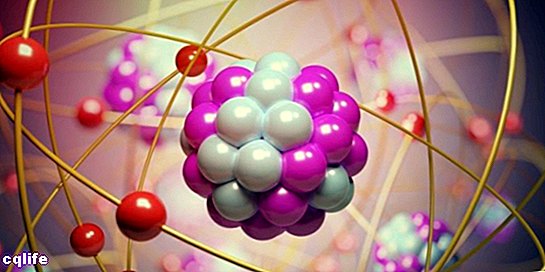
Atomy se skládají ze dvou základních částí:
- Jádro. Asi 99,94 % hmotnosti atomu je soustředěno v jádře, kde jsou protony a neutrony (které se společně nazývají „nukleony“), spojené silnými jadernými silami, které brání tomu, aby se protony vzájemně odpuzovaly a měly stejnou elektrickou energii. nabít.
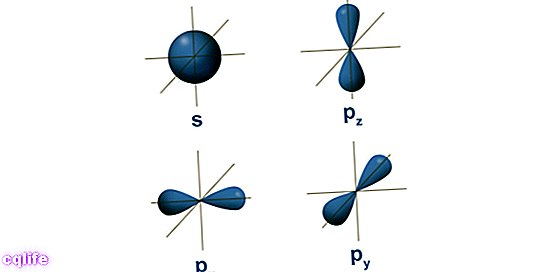
- Atomové orbitaly. Orbital popisuje prostorovou oblast obklopující atomové jádro, ve které je pravděpodobnost najít elektron je velmi vysoká. Tyto oblasti mají různé formy, které se získají jako výsledek řešení stacionární Schrödingerovy rovnice. Erwin Schrödinger byl rakouský vědec, který tuto rovnici vyvinul v roce 1925 pro výpočet vývoje subatomární částice, jako jsou elektrony. Elektrony tedy kolem jádra tvoří jakýsi „oblak“, který je reprezentován tvarem atomových orbitalů. Na druhou stranu každý atomový orbital odpovídá určité energetické hodnotě pro elektrony, takže jsou organizovány podle svých energetických hodnot. Následující obrázek ukazuje tvary prvních atomových orbitalů:
Historie atomu

První, kdo formuloval myšlenku existence atomů, byl řecký filozof Democritus (s.V-VI př. n. l.) z čistě smyšlených spekulací (jak byla tehdy věda chápána).
Jeho studiem se ujali pozdější filozofové jako Leucippus a Epikuros, ale během r. středověký, zastíněný kreacionistickým vysvětlením světa, který vše přisuzoval Bohu.
Museli jsme počkat až do roku 1773, kdy francouzský chemik Antoine de Lavoisier postuloval svou teorii o nestvoření nebo zničení hmoty (jen přeměňuje), resp. Zákon zachování hmoty, který umožnil Johnu Daltonovi v roce 1804 formulovat první moderní atomovou teorii.
Postupní učenci z fyzický a chemie byli inspirováni jeho prací, aby navrhli lepší a složitější systémy pro pochopení základních částic hmoty. Následně byly navrženy nové atomové modely až po ty nejpoužívanější dnes.
Současná přijímaná struktura je odvozena od experimenty z Rutherfordu v roce 1911 spolu s formulacemi Nielse Bohra, Schrödingera a Heisenberga.
Molekula
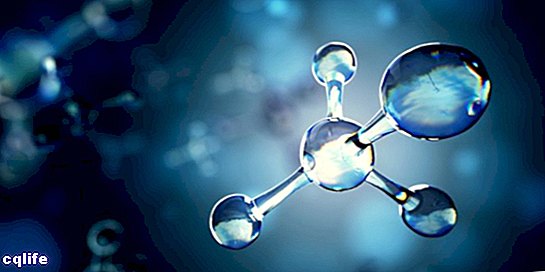
Molekula je známá jako spojení dvou nebo více atomů prostřednictvím chemických vazeb za vzniku složitější a elektricky neutrální struktury. Chemické vazby mohou být kovalentní nebo iontové.
Molekuly se mohou skládat z atomů stejného chemického prvku, například molekuly kyslíku (O2), nebo z atomů různých chemických prvků, například molekuly glukózy. Monatomické plyny, například helium (He), jsou také považovány za molekuly.

